Co to jest głęboka stymulacja mózgu?
Głęboka stymulacja mózgu (ang. deep brain stimulation – DBS) to metoda leczenia choroby Parkinsona, która polega na wszczepieniu cienkich elektrod stymulujących do głęboko położonych części mózgu.
Metoda ta należy do tzw. zabiegów stereotaktycznych, które wymagają użycia specjalnej ramy – urządzenia umożliwiającego precyzyjne wprowadzenie elektrody po ściśle określonej linii (tzw. trajektorii). Zabiegi te stają się coraz bardziej popularne; są wykonywane nie tylko w chorobie Parkinsona, lecz także w wielu innych zaburzeniach ruchowych, takich jak drżenie samoistne czy dystonia.
Obecnie na świecie ze stymulatorem mózgu żyje około 130 tys. osób. Pierwszy zabieg DBS w chorobie Parkinsona przeprowadzono w 1993 roku we Francji. Wkrótce potem zaczęto go stosować w innych krajach, w tym w Polsce. Obecnie DBS jest metodą zalecaną wszystkie neurologiczne towarzystwa naukoprzezwe do leczenia zaawansowanej choroby Parkinsona.
Jak działa stymulator mózgu?
Wszczepione elektrody generują impulsy elektryczne modyfikujące działanie ośrodków nerwowych odpowiedzialnych za rozwój choroby. Umieszczona w ciele pacjenta bateria (generator impulsów) zapewnia stałe źródło prądu (ryc. 1). Parametry wykorzystywanego prądu są bardzo niskie, a jego napięcie rzadko przekracza 4 V.
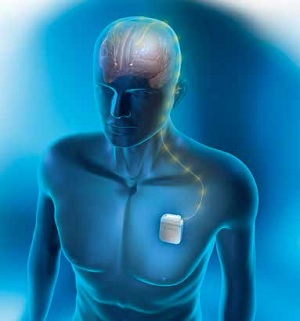
Ryc. 1. Stymulator umieszczony pod skórą klatki piersiowej generuje impulsy elektryczne, które płyną łącznikiem do elektrod umieszczonych głęboko w mózgu
Wybór miejsca umieszczenia elektrody (tzw. celu operacyjnego) zależy od obrazu klinicznego choroby, przewagi drżenia lub sztywności, a także obecności dodatkowych ruchów mimowolnych.
W chorobie Parkinsona elektrody wszczepia się najczęściej do niewielkiego miejsca w mózgu zwanego jądrem niskowzgórzowym (ang. subthalamic nucleus – STN), rzadziej do części wewnętrznej gałki bladej (ang. internal globus pallidus – GPI) lub jądra brzusznego pośredniego wzgórza (ang. ventral intermediate nucleus – VIN).
Co ciekawe, elektrody mózgowej nie wszczepia się do istoty czarnej – miejsca, gdzie w chorobie Parkinsona zanikają neurony dopaminowe – ponieważ wbrew nazwie głęboka stymulacja mózgu powoduje zahamowanie wybranych struktur nerwowych, a nie ich pobudzanie. Wszczepienie elektrody do istoty czarnej odniosłoby zatem odwrotny skutek. W warunkach fizjologicznych dopamina utrzymuje w równowadze pozostałe ośrodki nerwowe i hamuje niektóre z nich (np. STN). W chorobie Parkinsona, przy braku dopaminy, dochodzi więc do nadmiernego „odhamowania” niektórych struktur, wskutek czego pojawiają się objawy ruchowe (sztywność, drżenia, dyskinezy). Głęboka stymulacja mózgu przywraca równowagę w ośrodkach mózgowych, łagodząc objawy choroby Parkinsona.
Jak zbudowany jest stymulator mózgu i gdzie jest umieszczony?
Stymulator mózgu jest bardzo podobny do kardiostymulatora; różnica polega na tym, że elektrody umieszczone są w mózgu, a nie w sercu. Urządzenie składa się z generatora impulsów, czyli baterii, połączonej z elektrodą mózgową specjalnym przewodem (łącznikiem). Elektroda umieszczona jest w mózgu, przewód łączący znajduje się pod skórą na szyi, a generator impulsów jest położony w okolicy obojczyka i klatki piersiowej, również pod skórą. W Polsce stosowane są systemy DBS produkowane przez firmy: Medtronic, St. Jude Medical oraz Boston Scientific. Ogólna zasada działania stymulatorów jest taka sama, a różnice wynikają z technologii opracowania baterii, elektrod oraz systemu do programowania stymulatora.
System DBS jest niewidoczny, ale może być wyczuwalny pod skórą. Stymulator DBS pokazany na rycinie 15. to najczęściej wszczepiany w Polsce model Activa SC firmy Medtronic, o wymiarach 55 × 60 × 11 mm. Jest to bardzo lekki, ważący tylko 45 gramów jeden generator impulsów połączony jest jednym łącznikiem z pojedynczą elektrodą domózgową. Stymulator Vercise firmy Boston Scientific jest nieco mniejszy, o wymiarach 55 × 45 × 11 mm, natomiast stymulator Libra firmy St. Jude Medical ma wymiary 50 × 54 × 16 mm.
Elektrody domózgowe są stale udoskonalane. Obecnie stosowane są elektrody mające 4 lub 8 kontaktów, z których każdy może być aktywny. Stymulacja z każdego kontaktu może się charakteryzować odmiennymi parametrami prądu elektrycznego, co umożliwia precyzyjne dostosowanie terapii do poszczególnych pacjentów. Dodatkowo elektrody kierunkowe pozwalają na skoncentrowanie pola stymulacji nawet do niewielkiego, wybranego fragmentu struktury anatomicznej.
Jeśli u pacjenta występują obustronne objawy parkinsonowskie, konieczne jest założenie dwóch stymulatorów – jeden stymulator działa bowiem tylko na jedną (przeciwną) stronę ciała. W praktyce oznacza to konieczność przeprowadzenia dwóch operacji, z reguły w krótkim odstępie czasu. Istnieją tzw. stymulatory dwukanałowe, w których jedna bateria połączona jest z dwiema elektrodami. Można je wszczepić podczas jednej operacji. Obecnie w Polsce refundacją objęte są jedynie stymulatory jednokanałowe i takich się najczęściej używa.
Zasadniczą zaletę terapii DBS stanowi jej odwracalność, czyli przede wszystkim możliwość zmiany parametrów stymulacji, włączenia i wyłączenia urządzenia, a także w razie potrzeby całkowitego usunięcia systemu. Zmiany ustawień stymulatora dokonuje lekarz za pomocą specjalnego urządzenia do programowania.
Pacjent dysponuje natomiast pilotem służącym do obsługi stymulatora. Można nim włączać i wyłączać stymulator, a także zmieniać parametry prądu w granicach, które ustawił lekarz.
Dla kogo jest przeznaczona głęboka stymulacja mózgu?
DBS jest przeznaczona do leczenia pacjentów z zaawansowaną chorobą Parkinsona. Zastosowanie jej należy rozważyć w momencie, gdy u chorego pojawiły się powikłania ruchowe – stany zmiennej sprawności w ciągu dnia (naprzemiennie stan ON i OFF) – lub występują ruchy mimowolne (dyskinezy) ograniczające funkcjonowanie. Jeśli nie udaje się opanować tej sytuacji za pomocą farmakoterapii, najlepszym rozwiązaniem jest DBS. Cel operacyjny stanowi wówczas jądro niskowzgórzowe (DBS–STN) – „złoty standard” postępowania.
Zabieg wykonuje się też w przypadku znacznie nasilonego drżenia, niepoddającego się farmakoterapii, nawet jeśli inne objawy choroby Parkinsona nie są dla chorego zbyt uciążliwe. Wówczas nie zawsze stwierdza się dyskinezy. Cel operacyjny stanowi wzgórze (DBS–VIM) lub jądro niskowzgórzowe (DBS–STN).
Gdy u chorego występują bardzo nasilone dyskinezy, ruchy pląsawicze lub przetrwałe skręcające ruchy – tzw. dyskinezy dystoniczne – celem operacyjnym może być gałka blada (DBS–GPI).
O wyborze celu operacyjnego decydują wspólnie neurolog i neurochirurg.
Czy zabieg głębokiej stymulacji mózgu jest skuteczny?
Zabieg DBS–STN w chorobie Parkinsona jest niezwykle efektywny. Pozwala na istotną poprawę sprawności ruchowej, zmniejszenie sztywności mięśni, drżenia rąk i spowolnienia ruchowego, a także redukcję dyskinez i okresów „wyłączeń”. W analizie obejmującej wiele badań dotyczących DBS w chorobie Parkinsona średnią poprawę sprawności ruchowej oceniono na poziomie 52%. Jest to wartość uśredniona na podstawie oceny neurologicznej chorych przed zabiegiem i po nim. Oceny efektu DBS dokonuje się także na podstawie analizy jakości życia chorych i ich codziennej aktywności; efekt DBS jest wówczas z reguły jeszcze większy. U wielu chorych DBS umożliwia zmniejszenie dawki lewodopy średnio o 62%. Jest to wartość uzyskana na podstawie analizy badań klinicznych i nie stanowi reguły. U niektórych chorych DBS można określić jako „wartość dodaną” do dotychczasowej farmakoterapii bez zmniejszania dawki lewodopy.
Chorzy poddani zabiegowi DBS podkreślają ogólną poprawę możliwości wykonywania wszystkich tych czynności, które przed zabiegiem były dla nich zbyt uciążliwe. Na przykład chory, który przed zabiegiem mógł pokonywać dystans kilkuset metrów, a choroba ograniczała jego inną aktywność, w tym zabawę z wnukami oraz wykonywanie codziennych prac domowych, po zabiegu bez problemu przemierza kilkukilometrowe trasy po lesie, opiekuje się wnukami, robi zakupy, spotyka się z rodziną. Efekt DBS najlepiej mierzyć właśnie przez porównanie możliwości chorego i jakość jego życia przed DBS i po nim.
Wielu pacjentów po kilku miesiącach czy latach od zabiegu nie pamięta tych najgorszych chwil z bezpośredniego okresu przed operacją. Czasem twierdzą, że nie widzą efektu działania stymulatora DBS, ponieważ nadal stosują lewodopę i to w porównywalnych dawkach. Efekt działania DBS dostrzegają dopiero po wyłączeniu stymulatora, gdy doświadczą dawno już nieodczuwanego drżenia czy sztywności. Na pytanie, jak wyglądało ich życie przed wszczepieniem stymulatora, i czy chcieliby do niego wrócić, chorzy z reguły odpowiadają, że nie wyobrażają sobie powrotu do tamtych dni.
Każdy człowiek choruje inaczej. Nie ma też dwóch pacjentów z chorobą Parkinsona, u których kompilacja objawów ruchowych i pozaruchowych jest identyczna. Każdy ma inną osobowość, nastawienie, oczekiwania, sytuację rodzinną, społeczną czy zawodową. Dla każdego więc DBS oznacza inny efekt kliniczny w wymiarze ogólnoludzkim. Należy pamiętać, że korzyść z tego rodzaju leczenia jest bezwzględnie uwarunkowana właściwą kwalifikacją chorych do zabiegu. Zabieg DBS wiąże się bowiem nie tylko ze spodziewanymi korzyściami, lecz także z potencjalnym ryzykiem wystąpienia skutków ubocznych.
Jak długo działa DBS? Czy efekt jego działania może się wyczerpać?
Prawidłowo zakwalifikowany i zoperowany pacjent może się spodziewać długofalowego, stabilnego efektu DBS. Korzyść z tego zabiegu pozostawała na tym samym poziomie w ciągu 5-letniej obserwacji. Pomimo postępu choroby działanie DBS utrzymuje się, a możliwość modyfikacji parametrów stymulacji pozwala na kontrolę objawów ruchowych.
Jaki jest czas działania baterii stymulatora DBS?
Bateria stymulatora nieładowalnego wystarcza na 3–9 lat terapii. Jest to uzależnione od modelu stymulatora i parametrów prądu koniecznego do kontroli objawów ruchowych. Bateria nigdy nie wyczerpuje się z dnia na dzień. Za pomocą programatora lekarza i pilota pacjenta można sprawdzić jej stan. Gdy poziom baterii jest niski, chory zgłasza się ponownie na oddział neurochirurgii, gdzie w znieczuleniu miejscowym wyjmuje się starą baterię i wkłada nową. Wymiana dotyczy tylko baterii, a nie całego systemu. Elektrody domózgowe i przewód łączący pozostają na swoich miejscach, te elementy nie podlegają wymianie.
Stymulatory ładowalne mają baterię, którą można przezskórnie uzupełnić, a czas ich działania wynosi nawet 25 lat. Takich baterii nie trzeba wymieniać.


















